阅读时间大约6分钟(2341字)
阅读时间大约6分钟(2341字)
2025-07-22 牛津大学最新综述揭示组织工程与生物机器人的双向奔赴
出品:CAAI认知系统与信息处理专委会
在科幻电影中,我们经常看到拥有生物组织的机器人,它们既有机械的精准,又有生物的灵活。如今,这样的场景正在从幻想走向现实。
最近,牛津大学研究团队以“Skeletal Muscle Tissue Engineering: From TissueRegeneration to Biorobotics”为题,在中国科技期刊卓越行动计划二期英文梯队期刊Cyborg and Bionic Systems上发表综述文章,详细阐述了骨骼肌组织工程如何从最初的医疗需求,逐步演变成推动生物机器人发展的关键技术。这项研究不仅关乎如何修复受损的肌肉组织,更展现了工程化肌肉在机器人领域的巨大潜力。

从医疗需求到技术突破:骨骼肌工程的双重使命
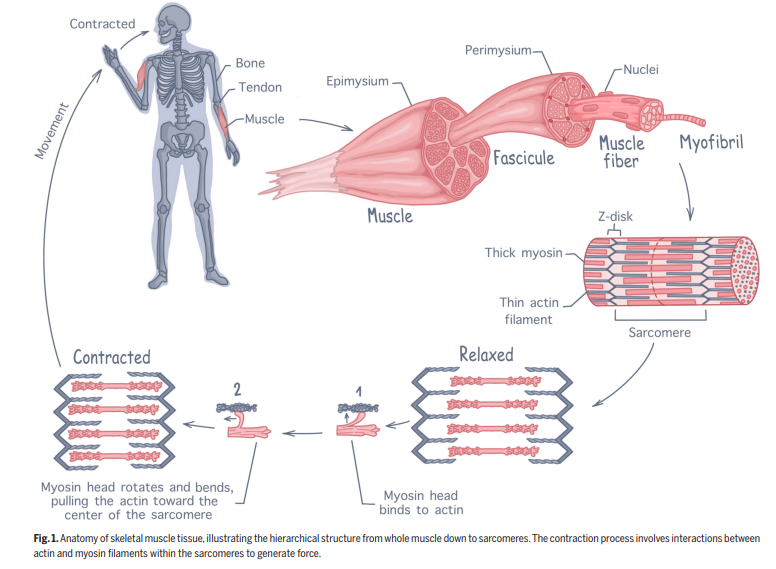
人体骨骼肌占体重的40%以上,是我们能够自如活动的关键。虽然肌肉具有惊人的自我修复能力,但当损失超过15%-20%时,就会形成永久性的功能丧失。目前的治疗方案主要依赖自体肌肉移植,但这种方法存在供体部位有限、手术创伤大、功能恢复不理想等诸多问题。
正是这种临床需求推动了骨骼肌组织工程的发展。研究人员试图在体外培养出功能性的肌肉组织,用于修复大面积肌肉缺损。然而,在这个过程中,科学家们意外发现了一个更广阔的应用领域——生物机器人。
骨骼肌作为天然的驱动系统,具有机械顺应性大、能量效率高、精细运动控制能力强等独特优势。更重要的是,它还能通过训练进行适应性调整。这些特性让工程化肌肉成为下一代软体机器人理想的驱动器。
研究团队指出,骨骼肌组织工程的核心策略包括四个关键要素:支架设计、细胞来源、外部刺激和生物反应器技术。每个要素都在不断创新,推动着这个领域向前发展。
支架与细胞:构建人工肌肉的基础架构
在组织工程中,支架就像建筑物的钢筋框架,为细胞生长提供三维支撑。理想的肌肉组织支架需要满足多项严苛要求:生物相容性好、降解速率与组织再生速度匹配、硬度接近天然肌肉(10-20 kPa)、能促进肌细胞的生长和排列。
研究人员探索了多种材料和制造技术。在材料选择上,既有合成聚合物如聚己内酯(PCL)、聚乳酸-羟基乙酸共聚物(PLGA),也有天然材料如纤维蛋白、胶原蛋白、海藻酸盐等。更有创新者利用脱细胞的植物组织(如白芦笋、苹果片)作为支架,展现了跨界思维的魅力。
制造技术同样百花齐放。静电纺丝技术可以制造出纳米级的纤维结构,精确控制纤维的直径和排列方向;3D生物打印技术能够逐层构建复杂的三维结构,将细胞、生物材料和生长因子精准定位;水凝胶微成型技术则通过软光刻制造出具有微米级表面图案的支架,引导细胞定向生长。
在细胞选择方面,研究面临着效果与伦理的双重考量。卫星细胞作为肌肉的天然干细胞,分化效果最好,但获取过程创伤大;间充质干细胞容易获得但分化能力有限;诱导多能干细胞(iPSCs)具有无限增殖和分化潜力,但存在致瘤风险。目前,大多数研究仍在使用小鼠C2C12肌母细胞系进行概念验证,距离临床应用还有一定距离。
刺激与培养:让人工肌肉"活"起来
仅有支架和细胞还不够,要让工程化的肌肉真正具备功能,需要模拟体内的生理环境,提供适当的刺激信号。研究发现,机械刺激、电刺激和生化刺激都对肌肉组织的成熟至关重要。
在机械刺激方面,基质硬度直接影响细胞分化方向。当培养基质的硬度在8-11 kPa(接近天然肌肉)时,肌细胞表现出最佳的肌节组织和收缩功能。动态拉伸也能促进肌纤维的排列和成熟,研究显示35%的应变率能达到最佳效果,这恰好与天然肌肉在收缩时的形变程度相符。
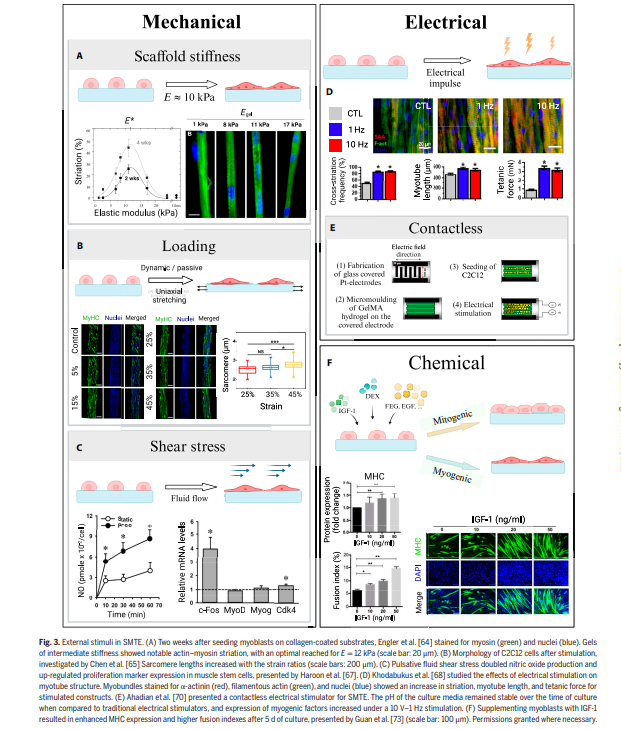
电刺激模拟了运动神经元对肌肉的激活作用。间歇性电刺激(如每小时1Hz或10Hz刺激,间隔7小时休息)能显著增加肌管的横截面积和长度,提高葡萄糖消耗和乳酸生成,最终使收缩力提高3倍。为避免电极腐蚀和培养基pH变化,研究人员还开发了非接触式电刺激装置。
生化刺激主要通过添加生长因子实现。胰岛素样生长因子-1(IGF-1)是个特殊的存在,它既能促进肌细胞增殖,又能诱导终末分化,在肌肉发育中扮演关键角色。地塞米松等糖皮质激素也被证明能促进肌管形成。
为了提供这些复杂的刺激,生物反应器技术应运而生。从最简单的静态培养到搅拌式、旋转壁式、灌流式反应器,再到最新的柔性生物反应器,每一代技术都在努力更好地模拟体内环境。特别值得一提的是,研究人员开始尝试使用人形机器人作为生物反应器平台,利用机器人的关节运动为组织提供生理相关的机械刺激。
当肌肉驱动机器人:生物混合系统的崛起
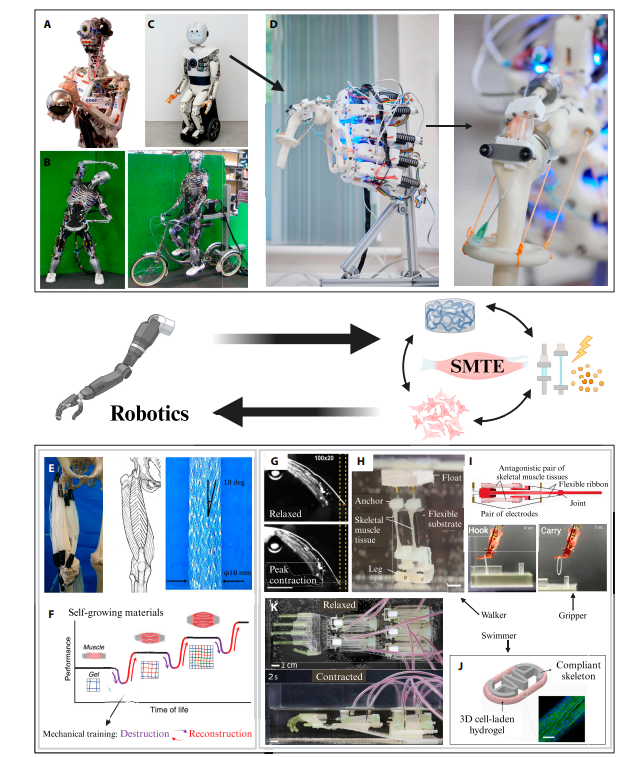
骨骼肌组织工程与机器人技术的结合,开辟了一个全新的研究领域——生物混合机器人。这些系统将工程化的肌肉组织作为驱动器,赋予机器人独特的优势。
与传统电机相比,肌肉驱动器具有多项优势:可以通过选择性激活不同的肌纤维束实现精细控制;具有内在的柔顺性,适合处理易碎物品;能够自主调节收缩力度,无需复杂的控制系统;理论上还可能具备自我修复和适应性生长的能力。
目前,研究人员已经开发出多种概念验证的肌肉驱动机器人。在微型尺度上,2D肌肉薄膜可以驱动悬臂梁结构产生弯曲变形,这类系统有望用于靶向药物递送。在较大尺度上,3D肌肉构建体已经成功驱动了抓取器、步行器和游泳器等装置。
一个特别引人注目的突破是,研究人员最近成功制造了一个18厘米高的生物混合手,能够选择性地移动单个手指并操纵物体。这是通过将长肌肉构建体并联成束来增加整体输出力实现的,为构建更大、更复杂的生物混合机器人开辟了道路。
控制这些生物驱动器同样充满挑战。除了传统的电刺激,研究人员正在探索光遗传学控制(通过基因修饰使肌肉对光敏感)、磁控制(利用磁性纳米粒子局部加热触发收缩)、化学控制(响应环境中的离子浓度变化)以及神经控制(构建神经-肌肉单元)等多种方法。
然而,要将这些概念推向实际应用,还需要克服诸多挑战。首当其冲的是血管化问题——没有血管网络,工程化肌肉的尺寸严重受限。其次是长期体外培养的挑战,需要在保持无菌环境的同时提供持续的营养供应。细胞来源也是个问题,需要找到既符合伦理要求又能大规模生产的细胞类型。
展望未来,骨骼肌组织工程正站在一个激动人心的十字路口。在医疗领域,它有望为肌肉缺损患者带来个性化的组织移植方案;在机器人领域,它可能催生出全新一代的软体驱动系统;在其他领域,如培养肉生产、药物筛选平台等也展现出巨大潜力。
正如研究团队所指出的,这个跨学科领域汇集了生物学、工程学和材料科学的智慧,正在产生有价值的新知识和创新。虽然前路仍有挑战,但持续的研究投入不仅是值得的,更是必要的。当生物与机械的界限变得模糊,一个充满无限可能的未来正在向我们走来。